|
| EL AGUA |
¿SABÍAS QUE?
- el agua cubre el 71% de la corteza terrestre
- el cuerpo humano tiene un 75% de agua al nacer y un 60% en la edad adulta.
- el 60% del agua que se encuentra en el cuerpo es intracelular; el resto circula por la sangre y tejidos.
- el ser humano no puede estar sin beber agua por mas de 5 o 6 días porque puede poner en peligro su vida.
ESTRUCTURA DEL AGUA.
 |
| Estructura molecular del agua. |
El oxígeno es mas electronegativo que el hidrógeno, teniendo la facultad de atraer mas fácil los electrones.
El agua es una molécula polar y presenta interacciones dipolo dipolo entre moléculas iguales, es decir, con H2O.
 |
| Formación de moléculas de H2O. |
PROPIEDADES DEL AGUA.
Propiedades Físicas. Propiedades Químicas.
- Estado Físico: Sólido, Líquido, Gaseoso. Reacciona con óxidos ácidos y básicos
- incolora Reacciona con metales y no metales
- insípida Forma hidratos con las sales
- inodora
- punto de congelación: 0°C
- punto de ebullición: 100°C
Propiedades mas importantes del agua:
 |
| Paso de estado sólido a líquido del agua. |
- elevado calor latente de vaporización.calor de vaporización: es la energía necesaria para pasar el agua de estado líquido a estado gaseoso.
- elevada temperatura de fusión y ebullición.
- elevado calor específico. Calor específico es la energía calórica necesaria para elevar la temperatura de un liquido a cierta cantidad.
- conductividad térmica.
- mayor densidad a 4°C que el hielo a 0°C.
- tensión superficial y capilaridad.
- conductividad eléctrica
- constante dialéctrica (E=80 a 25°C)
DISPERSIONES.
una dispersión es la unión de dos o mas sustancias en proporciones variables. Estas conservan sus propiedades químicas, las dispersiones se pueden separar por medios físicos. sus componentes se encuentran distribuidos uniformemente. Existen varios tipos de dispersiones:
Se define ósmosis como una difusión pasiva, caracterizada por el paso del agua, disolvente, a través de una membrana semipermeable, de la solución mas diluida a la mas concentrada.
- Homogéneas: se conocen mas como soluciones, están compuestas por soluto y solvente, sus componentes no se pueden apreciar a simple vista, presentan un aspecto uniforme.
- Heterogeneas: formadas por dos o mas sustancias puras que conservan sus propiedades particulares, por lo que podemos distinguir a simple vista sus componentes. en estas se distinguen 4 tipos de mezclas:
- Coloides: formadas por dos fases in posibilidad de que se mezclen los componentes, como el sol penetrando las partículas permitiendo tanto que se vea las partículas como la trayectoria del sol.
- sol: estado diluído de la mezcla, no llega a ser líquido, como el caso de la mayonesa o las espumas.
- gel: estado con mayor cohesión que la mezcla anterior pero no llega a ser sólido, como la jalea.
- suspenciones: mezclas heterogéneas en las que un sólido se mezcla en un líquido.
DISOLUCIONES ACUOSAS.
Una disolución es una mezcla homogénea, cuyos componentes son solutos y disolventes.
la disolución se presenta cuando una sustancia se disuelve completamente en la otra.
en la disolución acuosa se da que el solvente o disolvente es agua y el soluto puede ser un sólido, un líquido o un gas.
Propiedades coligativas de las disoluciones:
son las propiedades que dependen mas de de la concentración de partículas de soluto. Algunas de ellas son:
son las propiedades que dependen mas de de la concentración de partículas de soluto. Algunas de ellas son:
- disminución de la presión de vapor
- presión osmótica
- aumento del punto de ebullición
- disminución del punto de congelación
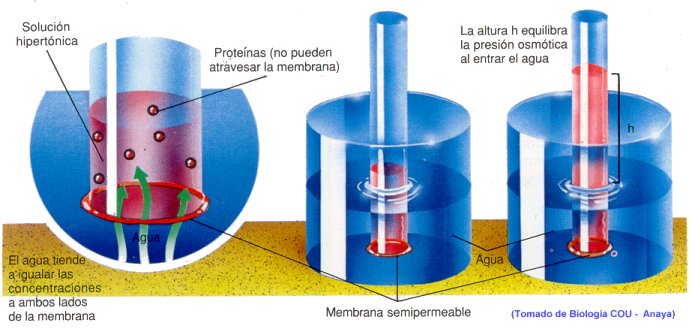
Ósmosis:
Se define ósmosis como una difusión pasiva, caracterizada por el paso del agua, disolvente, a través de una membrana semipermeable, de la solución mas diluida a la mas concentrada.
Presión osmótica: es la presión necesaria para detener el flujo del agua a través de la membrana semipermeable.
BIBLIOGRAFÍA
FUENTE ORAL: La fuente oral que utilicé para esta entrada fueron las clases de biología y las explicaciones por parte del profesor [Wilmer Soler. Profesor biologia de la célula I 2010/2]. Esperaba entender bien el tema ampliar un poco lo conocimientos previos que ya tenía. Las expectativas se cumplieron, se hizo una explicación completa acerca del tema.
FUENTE ESCRITA: Documento sobre el Agua.
se desconoce información acerca del titulo del libro del que fue sacado, su autor y editorial.
Capítulo 3. El Agua:El medio de la vida.
Documento suministrado a los estudiantes Primer semestre de Medicina Universidad CES por el Prof. Artenio Bogallo.
El anterior es un completo documento acerca del agua, su importancia en la vida y todo lo relacionado a su estructura y propiedades físicas y químicas.
FUENTE VIRTUAL:
Las siguientes son las fuentes consultadas para la realización de esta entrada:
Universidad de Murcia
Tecnológico
http://www.mitecnologico.com/Main/DispersionesOMezclasFortunecity
http://www.fortunecity.es/expertos/profesor/171/agua.html
Wikipedia
http://es.wikipedia.org/wiki/Agua
Universidad Nacional -Virtual
http://www.virtual.unal.edu.co/cursos/ciencias/2000051/lecciones/cap01/06_11.htm
Aula 21
http://www.aula21.net/Nutriweb/agua.htm